Zawartość
- Dziedziczny rak piersi
- Mutacje genów spoza BRCA
- Rak piersi i badania genetyczne
- Wsparcie dla dziedzicznego raka piersi
Oprócz mutacji genów BRCA1 i BRCA2, niektóre z nich obejmują mutacje w ATM, PALB2, PTEN, CDH1, CHEK2, TP53, STK11, PMS2 i innych. Przyjrzyjmy się, jak ważne są te mutacje inne niż BRCA1 / BRCA2 w rodzinnym raku piersi i niektórym cechom tych, które są częściej spotykane.
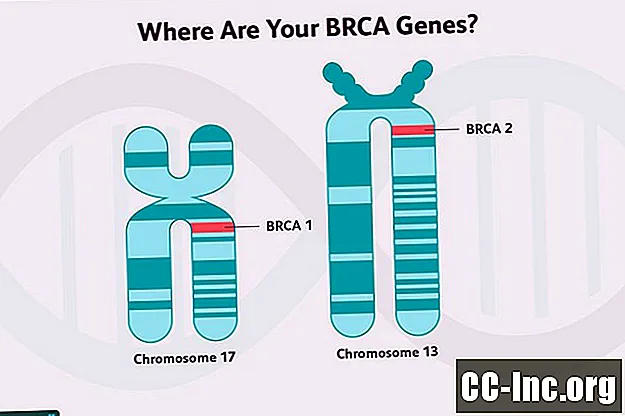
Dziedziczny rak piersi
Obecnie uważa się, że od 5 do 10 procent przypadków raka piersi jest genetycznych lub rodzinnych (chociaż liczba ta może się zmienić, gdy dowiemy się więcej), ale nie wszystkie te nowotwory są spowodowane mutacjami BRCA.
Co najwyżej 29 procent (i prawdopodobnie znacznie mniej) dziedzicznych raków piersi ma pozytywny wynik na mutacje genów BRCA1 lub BRCA2, a wiele osób prowadzi testy pod kątem innych znanych zmian genetycznych.
Ponieważ nauka stojąca za dziedzicznym rakiem wywołuje niepokój, nie mówiąc o zagmatwaniu i niekompletności, warto zacząć od omówienia biologii mutacji genów i tego, jak te zmiany w DNA odgrywają rolę w rozwoju raka.
Odziedziczone a nabyte mutacje genów
Mówiąc o mutacjach, ważne jest, aby odróżnić mutacje genetyczne odziedziczone od nabytych.
Nabyte lub somatyczne mutacje genów zyskały w ostatnich latach wiele uwagi, ponieważ mutacje te powodują zmiany, które napędzają rozwój raka. Terapie celowane, leki ukierunkowane na określone szlaki związane z tymi zmianami, znacznie poprawiły leczenie niektórych nowotworów, takich jak rak płuc.
Nabyte mutacje nie są jednak obecne od urodzenia, ale raczej powstają w dowolnym momencie po urodzeniu w procesie przekształcania się komórki w komórkę rakową. Mutacje te dotyczą tylko niektórych komórek ciała. Nie są dziedziczone od rodzica, ale raczej „nabywane”, ponieważ DNA w komórkach jest narażone na uszkodzenia ze środowiska lub w wyniku normalnych procesów metabolicznych organizmu.
Z kolei mutacje dziedziczone lub mutacje linii zarodkowej są zmianami genetycznymi, z którymi ludzie się rodzą i które są przekazywane przez jednego lub oboje rodziców. Te mutacje wpływają na wszystkie komórki ciała. To właśnie te odziedziczone mutacje (i inne zmiany genetyczne) mogą zwiększać ryzyko zachorowania na raka i odpowiadać za tak zwany dziedziczny lub rodzinny rak piersi.
Dziedziczne (zarodkowe) a nabyte (somatyczne) mutacje genówJak dziedziczne mutacje genów zwiększają ryzyko raka?
Wiele osób zastanawia się, w jaki dokładnie sposób nieprawidłowy gen lub kombinacja genów może prowadzić do raka piersi, a krótkie omówienie biologii jest pomocne w zrozumieniu wielu pytań, takich jak dlaczego nie u każdego, kto ma te mutacje, zachoruje na raka.
Nasze DNA to plan lub kod używany do produkcji białek. Kiedy mapa lub kod jest nieprawidłowy (np. „Liternictwo” w określonym genie), podaje niewłaściwe wskazówki dotyczące syntezy białka. Nieprawidłowe białko nie jest wtedy w stanie wykonywać swojej zwykłej pracy. Nie wszystkie mutacje genów zwiększają ryzyko raka, a większość z nich nie. Mutacje w genach odpowiedzialnych za wzrost i podział komórek, czyli „mutacje kierujące”, są tym, co napędza wzrost raka. Istnieją dwa główne typy genów, które zmutowane mogą prowadzić do niekontrolowanego wzrostu znanego jako rak: onkogeny i geny supresorowe.
Kilka genów związanych z wyższym ryzykiem raka piersi to geny supresorowe. Te geny kodują białka, które działają w celu naprawy uszkodzeń DNA w komórkach (uszkodzenia spowodowane toksynami w środowisku lub normalnych procesów metabolicznych w komórkach), służą do eliminacji komórek, których nie można naprawić, lub regulują wzrost w inny sposób. Geny BRCA1 i BRCA2 są genami supresorowymi nowotworów.
Wiele z tych genów jest autosomalnych recesywnych, co oznacza, że każda osoba dziedziczy jedną kopię genu od każdego z rodziców i obie kopie muszą zostać zmutowane, aby zwiększyć ryzyko raka. Upraszczając, oznacza to, że kombinacja czynników genetycznych i środowiskowych (nabyta mutacja w drugim genie) musi działać razem, aby spowodować rozwój raka. Do tego dochodzi zwykle kilku mutacji, aby komórka stała się komórką rakową.
Co to znaczy mieć genetyczne predyspozycje do rakaGene Penetrance
Nie wszystkie mutacje genów lub zmiany genetyczne zwiększają ryzyko raka piersi w takim samym stopniu, i jest to ważna koncepcja dla każdego, kto rozważa testy genetyczne, zwłaszcza że wiele osób słyszało o bardzo wysokim ryzyku związanym z mutacjami BRCA. Penetrację genów definiuje się jako odsetek osób z mutacją, u których wystąpi stan (w tym przypadku rak piersi).
W przypadku niektórych mutacji ryzyko raka piersi jest bardzo wysokie. W innych przypadkach ryzyko może wzrosnąć tylko o współczynnik 1,5. Ważne jest, aby to zrozumieć, mówiąc o możliwych opcjach zapobiegawczych.
Epigenetyka
Inną ważną koncepcją, która jest ważna dla zrozumienia genetyki i raka, choć jest zbyt złożona, aby ją tu szczegółowo zbadać, jest epigenetyka. Dowiedzieliśmy się, że zmiany w DNA, które nie obejmują zmian w parach zasad (nukleotydach) lub „literach” kodujących białko, mogą być równie ważne w rozwoju raka. Innymi słowy, zamiast zmian strukturalnych w kręgosłupie DNA mogą wystąpić zmiany molekularne, które zmieniają sposób odczytywania lub wyrażania wiadomości.
Mutacje genów spoza BRCA
Mutacje genu BRCA są najbardziej znanymi nieprawidłowościami genetycznymi związanymi z rakiem piersi, ale jest jasne, że są kobiety, które są predysponowane do raka piersi na podstawie historii rodzinnej, u których wynik testu jest ujemny.
Badanie z 2017 roku wykazało, że mutacje BRCA stanowią tylko 9 do 29 procent dziedzicznych raków piersi. Jednak nawet jeśli przeprowadzono testy dla kolejnych 20 do 40 znanych mutacji, tylko 4 do 11 procent kobiet uzyskało wynik pozytywny. Innymi słowy, od 64 do 86 procent kobiet podejrzewa się, że ma dziedzicznego raka piersi, z wynikiem ujemnym zarówno pod względem mutacji BRCA, jak i 20 do 40 innych.
Rodzinny rak piersi nie-BRCA1 / BRCA2
Nasza wiedza na temat mutacji genów, które zwiększają ryzyko raka piersi, jest wciąż niepełna, ale obecnie wiemy, że istnieją co najmniej 72 mutacje genów związane z dziedzicznym rakiem piersi. Uważa się, że te mutacje (i inne jeszcze nieodkryte) są odpowiedzialne za 70% do 90% dziedzicznych raków piersi, które mają negatywny wynik testu na mutacje genu BRCA. Akronim BRCAX został ukuty w celu opisania tych innych mutacji, oznaczając BRCA1 Rodzinny rak piersi związany z BRCA2.
72 Mutacje genetyczne związane z dziedzicznym rakiem piersiPoniższe nieprawidłowości genetyczne różnią się częstotliwością, stopniem związanego z nimi ryzyka, rodzajem raka piersi, z którym są powiązane oraz innymi nowotworami związanymi z mutacjami.
Większość z tych raków piersi ma cechy podobne (takie jak typ raka, status receptorów estrogenowych i status HER2) do niedziedzicznych lub sporadycznych raków piersi, ale są wyjątki. Na przykład niektóre mutacje są silniej związane z potrójnie ujemnym rakiem piersi, w tym mutacje w BARD1, BRCA1, BRCA2, PALB2, iRAD51D.
Zmienność w mutacjach
Nie wszyscy ludzie, którzy mają następujące mutacje genów, są tacy sami. Ogólnie rzecz biorąc, mogą istnieć setki sposobów mutacji tych genów. W niektórych przypadkach gen będzie wytwarzał białka hamujące wzrost guza, ale białka nie będą działać tak dobrze, jak normalne białko. W przypadku innych mutacji białko może w ogóle nie zostać wyprodukowane.
BRCA (krótki przegląd do porównania)
Mutacje genu BRCA 1 i mutacje genu BRCA2 są związane ze zwiększonym ryzykiem zachorowania na raka piersi, a także niektórych innych nowotworów, chociaż oba te rodzaje ryzyka nieco się różnią.
Średnio 72 procent kobiet z mutacjami BRCA1 i 69 procent ze zmutowanymi genami BRCA2 zachoruje na raka piersi w wieku 80 lat.
Ponadto raki piersi związane z tymi mutacjami mogą się różnić. Rak piersi u kobiet z mutacją BRCA1 ma większe prawdopodobieństwo potrójnie ujemnego wyniku. Około 75 procent ma ujemne receptory estrogenowe, a także rzadziej jest HER2-dodatnie. Jest również bardziej prawdopodobne, że mają wyższy stopień guza. Z kolei raki piersi u kobiet z mutacjami BRCA2 są podobne do nowotworów u kobiet, które nie są nosicielkami mutacji genu BRCA.
Gen ATM (kinaza serynowo / treoninowa ATM)
Gen ATM koduje białka, które pomagają kontrolować tempo wzrostu komórek. Pomagają również w naprawie uszkodzonych komórek (komórek, które doznały trwałego uszkodzenia DNA przez toksyny) poprzez aktywację enzymów, które naprawiają te uszkodzenia.
Ci, którzy mają dwie kopie zmutowanego genu, mają rzadki zespół autosomalny recesywny znany jako ataksja-teleangiektazja. W przypadku ataksji-teleangiektazji wadliwe białka nie tylko zwiększają ryzyko raka, ale także powodują zbyt szybkie obumieranie niektórych komórek w mózgu, co prowadzi do postępującego zaburzenia neurodegeneracyjnego.
Osoby, które mają tylko jedną zmutowaną kopię genu (około 1 procent populacji), mają od 20 do 60 procent ryzyka zachorowania na raka piersi w ciągu całego życia.
Uważa się, że osoby z tą mutacją są predysponowane do raka piersi w młodym wieku, a także do rozwoju obustronnego raka piersi.
Badania przesiewowe w kierunku raka piersi za pomocą rezonansu magnetycznego piersi są zalecane od 40 roku życia, a kobiety mogą chcieć rozważyć profilaktyczną mastektomię. Osoby z jednym zmutowanym genem ATM wydają się również mieć predyspozycje do raka tarczycy i trzustki oraz są bardziej wrażliwe na promieniowanie.
PALB2
Mutacje w genie PALB2 są również ważną przyczyną dziedzicznego raka piersi. Gen PALB2 koduje białko, które działa w połączeniu z białkiem BRCA2 w celu naprawy uszkodzonego DNA w komórkach. Ogólnie rzecz biorąc, ryzyko zachorowania na raka piersi z mutacją PALB2 w ciągu całego życia wynosi aż 58 procent, chociaż może się różnić w zależności od wieku. Ryzyko jest średnio od 8 do 9 razy większe w przypadku kobiet w wieku poniżej 40 lat, ale około 5 razy średnio w przypadku kobiet w wieku powyżej 60 lat.
Wśród tych, które mają jedną kopię genu, 14 procent zachoruje na raka piersi w wieku 50 lat i 35 procent w wieku 70 lat (mniej niż w przypadku mutacji BRCA).
Osoby, u których występuje mutacja PALB2 i zachorują na raka piersi, mogą mieć większe ryzyko zgonu z powodu tej choroby.
Ludzie, którzy dziedziczą 2 kopie zmutowanego genu PALB2, mają rodzaj anemii Fanconiego charakteryzujący się bardzo niską liczbą czerwonych krwinek, białych krwinek i płytek krwi.
CHEK2
Gen CHEK2 koduje białko, które jest aktywowane po uszkodzeniu DNA. Aktywuje również inne geny zaangażowane w naprawę komórek.
Ryzyko w ciągu całego życia nosicielek mutacji obcinających CHEK2 wynosi 20% dla kobiety bez chorego krewnego, 28% dla kobiety z chorym krewnym drugiego stopnia, 34% dla kobiety z jednym krewnym dotkniętym chorobą pierwszego stopnia i 44% dla kobieta z chorym krewnym pierwszego i drugiego stopnia.
Zarówno w przypadku mężczyzn, jak i kobiet gen zwiększa również ryzyko raka okrężnicy i chłoniaka nieziarniczego.
CDH1
Mutacje w CDH1 powodują stan znany jako dziedziczny zespół raka żołądka.
Osoby, które odziedziczyły ten gen, mają do 80% ryzyko zachorowania na raka żołądka i do 52% w przypadku raka zrazikowego piersi.
Gen koduje białko (kadherynę nabłonkową), które pomaga komórkom przylegać do siebie (jedną z różnic między komórkami nowotworowymi a normalnymi komórkami jest brak tych chemikaliów adhezyjnych, które powodują ich przyleganie). Nowotwory u osób, które dziedziczą tę mutację, są bardziej narażone na przerzuty.
PTEN
Mutacje w genie PTEN są jednymi z bardziej powszechnych mutacji genu supresorowego guza. Gen koduje białka, które regulują wzrost komórek, a także pomagają komórkom trzymać się razem.
Wydaje się, że mutacje w genie zwiększają ryzyko oderwania się komórek rakowych od guza i przerzutów. PTEN jest związany z zespołem zwanym guzem hamartoma PTEN, a także zespołem Cowdena.
Kobiety, które są nosicielami mutacji PTEN, są narażone na ryzyko zachorowania na raka piersi nawet do 85 procent, a także mają zwiększone ryzyko łagodnych zmian piersi, takich jak choroba włóknisto-torbielowata, adenoza i brodawczakowatość wewnątrzprzewodowa.
Mutacje są również powiązane ze zwiększonym ryzykiem raka macicy (i łagodnych mięśniaków macicy), raka tarczycy, raka okrężnicy, czerniaka i raka prostaty.
Objawy niezwiązane z rakiem obejmują duży rozmiar głowy (makrocefalia) i skłonność do tworzenia łagodnych guzów zwanych hamartoma.
STK11
Mutacje w STK11 są związane z chorobą genetyczną znaną jako zespół Peutza-Jeghera. STK11 jest genem supresorowym guza zaangażowanym we wzrost komórek.
Oprócz zwiększonego ryzyka raka piersi (z ryzykiem życiowym sięgającym nawet 50 procent), zespół ten niesie zwiększone ryzyko wielu nowotworów, z których niektóre obejmują raka okrężnicy, raka trzustki, raka żołądka, raka jajnika, raka płuc, rak macicy i nie tylko.
Stany niezwiązane z rakiem związane z mutacją obejmują nienowotworowe polipy w przewodzie pokarmowym i układzie moczowym, piegi na twarzy i wnętrzu jamy ustnej i inne. Badania przesiewowe w kierunku raka piersi są często zalecane kobietom w wieku od 20 lat i często z MRI z lub bez mammografii.
TP53
Gen TP53 koduje białka, które hamują wzrost nieprawidłowych komórek.
Te mutacje są niezwykle powszechne w przypadku raka z nabyty mutacje w genie p53 występują w około 50 procentach przypadków raka.
Mutacje dziedziczne są mniej powszechne i są związane ze stanami znanymi jako zespół Li-Fraumeni lub zespół podobny do Li-Fraumeni (który ma mniejsze ryzyko raka). Większość osób, które odziedziczyły mutację, zachoruje na raka w wieku 60 lat, a oprócz raka piersi jest podatna na raka kości, raka nadnerczy, raka trzustki, raka okrężnicy, raka wątroby, guzy mózgu, białaczkę i inne. Nierzadko zdarza się, że osoby z mutacją zapadają na więcej niż jeden pierwotny nowotwór.
Uważa się, że odziedziczone mutacje w genie p53 odpowiadają za około 1 procent przypadków dziedzicznego raka piersi. Raki piersi związane z mutacją są często HER2 dodatnie i mają wysoki stopień złośliwości.
Syndrom Lyncha
Zespół Lyncha lub dziedziczny rak jelita grubego niezwiązany z polipowatością jest związany z mutacjami w kilku różnych genach, w tym PMS2, MLH1, MSH2, MSH6 i EPCAM.
W szczególności PMS2 wiąże się z podwójnym ryzykiem raka piersi. Gen działa jako gen supresorowy guza, kodując białko, które naprawia uszkodzony DNA.
Oprócz raka piersi mutacje te niosą ze sobą wysokie ryzyko raka okrężnicy, jajnika, macicy, żołądka, wątroby, pęcherzyka żółciowego, jelita cienkiego, nerek i mózgu.
Inne mutacje
Istnieje kilka innych mutacji genów związanych ze zwiększonym ryzykiem zachorowania na raka piersi i oczekuje się, że w najbliższej przyszłości zostanie odkrytych więcej. Niektóre z nich obejmują:
- BRIP1
- BARD1
- MRE11A
- NBN
- RAD50
- RAD51C
- SEC23B
- BLM
- MUTYH
Rak piersi i badania genetyczne
W chwili obecnej dostępne są testy mutacji genów BRCA, a także mutacji ATM, CDH1, CHEK2, MRE11A, MSH6, NBN, PALB2, PMS2, PTEN, RAD50, RAD51C, SEC23B i TP53, przy czym spodziewany jest wzrost tego obszaru dramatycznie w najbliższej przyszłości.
Jednak posiadanie tych testów rodzi wiele pytań. Na przykład, kto może mieć dziedzicznego raka piersi i kto powinien zostać przebadany? Co powinieneś zrobić, jeśli wynik testu na jeden z tych genów jest pozytywny?
W idealnym przypadku wszelkie testy powinny być wykonywane wyłącznie pod kierunkiem i pomocą doradcy genetycznego. Są ku temu dwa powody.
Jednym z nich jest to, że może być katastrofalne, gdy dowiesz się, że nosisz mutację, która może zwiększyć Twoje ryzyko, a wskazówki osoby, która jest świadoma zalecanego postępowania i badań przesiewowych, są nieocenione.
Jak wspomniano wcześniej, niektóre mutacje wiążą się z wysokim ryzykiem, a inne znacznie niższe. Niektóre mutacje mogą budzić większe obawy we wcześniejszym życiu (powiedzmy, w wieku 20 lat), podczas gdy inne mogą nie wymagać wczesnego badania przesiewowego. Doradca genetyczny może pomóc Ci dowiedzieć się, jakie są obecnie zalecenia dotyczące badań przesiewowych pod kątem konkretnej mutacji, biorąc pod uwagę wszelkie inne czynniki ryzyka, które możesz mieć.
Innym powodem, dla którego poradnictwo genetyczne jest tak ważne, jest znaczne ryzyko zachorowania na raka piersi, nawet jeśli wyniki testów są ujemne. Jest jeszcze wiele do nauczenia się, a doradca genetyczny może pomóc Ci przyjrzeć się historii Twojej rodziny, aby sprawdzić, czy pomimo negatywnych testów możesz być obciążony wysokim ryzykiem, i odpowiednio zaplanować badania przesiewowe.
Badania genetyczne w kierunku raka piersiWsparcie dla dziedzicznego raka piersi
Tak jak ludzie, u których zdiagnozowano raka piersi, potrzebują wsparcia, ci, którzy mają geny zwiększające ryzyko, potrzebują wsparcia. Na szczęście istnieją organizacje, które koncentrują się szczególnie na wspieraniu ludzi w tej sytuacji.
Jedna organizacja, FORCE, to skrót od Facing Our Risk of Cancer Empowered, oferuje infolinię, tablicę ogłoszeń i informacje dla osób zmagających się z dziedzicznym rakiem.
Dostępne są inne organizacje i społeczności wspierające, które pomagają ludziom w podejmowaniu decyzji związanych z rozpoznaniem dziedzicznego raka piersi.
Termin „osoba, która przeżyła” została wymyślona przez FORCE, aby opisać ludzi, którzy przeżywają predyspozycje do raka piersi. Jeśli taka jest sytuacja, z którą masz do czynienia, nie jesteś sam, a używając hashtagu #previvor, możesz znaleźć wiele innych osób na Twitterze i innych portalach społecznościowych.
Słowo od Verywell
Poznanie wielu różnych mutacji genów, które zwiększają ryzyko raka piersi poza mutacje BRCA, może być przytłaczające, ale te „inne” mutacje mają istotne znaczenie, wiedząc, że mutacje BRCA stanowią względną mniejszość rodzinnych nowotworów piersi. Jednocześnie nauka zajmująca się dziedzicznym rakiem piersi jest wciąż w powijakach i można się wiele nauczyć. Jeśli obawiasz się, że możesz mieć mutację lub dowiedziałeś się, że tak jest, warto dowiedzieć się jak najwięcej. Organizacje zajmujące się rakiem dziedzicznym, takie jak FORCE, mogą nie tylko udzielić dalszych informacji, ale mogą pomóc w nawiązaniu kontaktu z innymi osobami, które stoją przed podróżą z podobnymi pytaniami i obawami.