Zawartość
- Co to jest HHT?
- Kogo to dotyczy?
- Diagnoza
- Rodzaje
- Monitorowanie i zapobieganie
- Zabiegi badawcze
- Ekranizacja
Możliwe jest również, aby mieć HHT i nie wiedzieć, że go masz, a niektóre osoby są po raz pierwszy diagnozowane po wystąpieniu poważnych powikłań związanych z HHT. Prawie 90% osób z HHT będzie miało nawracające krwawienia z nosa, ale stosunkowo częste są również poważniejsze powikłania. Poważne komplikacje zależą po części od umiejscowienia nieprawidłowych naczyń krwionośnych i obejmują wewnętrzne krwawienie i udar, ale HHT może również milczeć przez lata.
Co to jest HHT?
HHT jest chorobą dziedziczną, która wpływa na naczynia krwionośne w sposób, który może powodować nieprawidłowości, od bardzo niewinnych do potencjalnie zagrażających życiu, gdy spojrzymy na całe życie. Chociaż oznaki i objawy mogą pojawić się wcześnie, często jest tak, że poważniejsze powikłania mogą pojawić się dopiero po 30 roku życia.
Istnieją dwa główne typy zaburzeń naczyń krwionośnych, które mogą wpływać na osoby z HHT:
- Telangiectasias
- Tętniczomalformacje lub AVM.
Telangiectasia
Termin teleangiektazja odnosi się do grupy małych naczyń krwionośnych (naczyń włosowatych i małych żyłek), które zostały nieprawidłowo rozszerzone. Chociaż teleangiektazje mogą powstawać we wszystkich różnych częściach ciała, najłatwiej jest je dostrzec i najczęściej uważa się je za pojawiające się blisko powierzchni skóry, często na twarzy lub na udach, czasami określane jako „pajączki”. lub „pęknięte żyły”.
Można je również zobaczyć na wilgotnych błonach śluzowych lub wyściółkach, takich jak wnętrze jamy ustnej, policzki, dziąsła i usta. Mają czerwony lub purpurowy odcień i wyglądają jak kręte, żylaste nitki lub pajęcze sieci.
Wpływ i zarządzanie teleangiektazją
Teleangiektazje skóry i błon śluzowych (wilgotna wyściółka jamy ustnej i warg) są powszechne wśród pacjentów z HHT. Teleangiektazje zwykle pojawiają się, gdy osoba jest młoda i postępuje wraz z wiekiem. Krwawienie może wystąpić z tych miejsc, ale zwykle jest łagodne i łatwe do opanowania. W razie potrzeby stosuje się czasem ablację laserową.
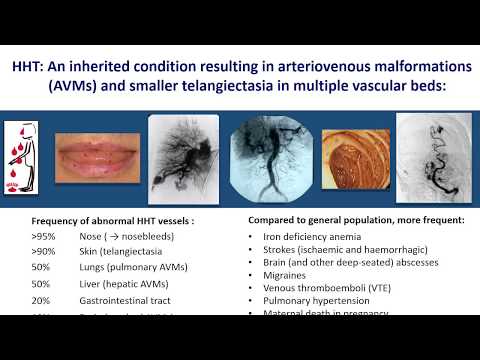
Teleangiektazje nosa - w wyściółce dróg oddechowych - to powód, dla którego krwawienia z nosa są tak częste u osób z HHT. Około 90% osób z HHT ma nawracające krwawienia z nosa. Krwawienia z nosa mogą być łagodne lub cięższe i nawracać, co prowadzi do niedokrwistości, jeśli nie są kontrolowane. U większości osób z HHT krwawienie z nosa rozwija się przed 20 rokiem życia, ale wiek zachorowania może się znacznie różnić, podobnie jak nasilenie choroby.
W przewodzie pokarmowym teleangiektazje występują u około 15 do 30% osób z HHT. Mogą być źródłem krwawienia wewnętrznego, jednak rzadko zdarza się to przed 30 rokiem życia. Leczenie różni się w zależności od ciężkości krwawienia i indywidualnego pacjenta. Uzupełnienie żelaza i transfuzje w razie potrzeby mogą być częścią planu; Terapia estrogenowo-progesteronowa i terapia laserowa mogą być stosowane w celu zmniejszenia nasilenia krwawienia i potrzeby transfuzji.
Malformacje tętniczo-żylne (AVM)
Malformacje tętniczo-żylne lub AVM reprezentują inny rodzaj wad rozwojowych naczyń krwionośnych, często występujących w ośrodkowym układzie nerwowym, płucach lub wątrobie. Mogą być obecne przy urodzeniu i / lub rozwijać się z czasem.
AVM są uważane za wady rozwojowe, ponieważ naruszają uporządkowaną sekwencję, którą normalnie podążają naczynia krwionośne, dostarczając tlen do tkanek i przenosząc dwutlenek węgla z powrotem do płuc w celu wydychania: natleniona krew normalnie przepływa z płuc i serca, przez aortę do od największej z tętnic, do mniejszych tętnic do tętniczek, a nawet mniejszych tętniczek ostatecznie do najmniejszych z mniejszych naczyń włosowatych; następnie odtleniona krew przepływa przez małe żyłki do małych żył, do większych żył, aby ostatecznie do wielkich żył, takich jak żyła główna górna, iz powrotem do serca itp.
W przeciwieństwie do tego, gdy rozwija się AVM, dochodzi do nieprawidłowego „splątania” naczyń krwionośnych łączących tętnice z żyłami w określonej części ciała, co może zakłócać normalny przepływ krwi i krążenie tlenu. To prawie tak, jakby międzystanowa autostrada nagle opuściła parking, po czym samochody przez chwilę wirują, zanim wrócą na międzystanową, być może w złym kierunku.
Wpływ i zarządzanie AVM
U osób z HHT AVM mogą wystąpić w płucach, mózgu i ośrodkowym układzie nerwowym oraz krążeniu wątroby. AVM mogą pękać, powodując nieprawidłowe krwawienie, prowadzące do udaru, krwawienia wewnętrznego i / lub ciężkiej anemii (niewystarczająca ilość zdrowych czerwonych krwinek, powodująca zmęczenie, osłabienie i inne objawy).
Kiedy AVM tworzą się w płucach u osób z HHT, stan może nie uzyskać pomocy medycznej, dopóki dana osoba nie osiągnie 30 lat lub więcej. Osoba może mieć AVM w płucach i nie wiedzieć o tym, ponieważ nie ma żadnych objawów. Alternatywnie, osoby z AVM płuc mogą nagle rozwinąć masywne krwawienie, odkrztuszanie krwi. AVM płuc może również powodować cichsze szkody, przez co dostarczanie tlenu do organizmu jest poniżej normy, a osoba ma wrażenie, że nie może uzyskać wystarczającej ilości powietrza, leżąc w łóżku w nocy (ten objaw jest częściej spowodowany nie związanymi z HHT stanach, takich jak niewydolność serca). Coś zwanego paradoksalnymi zatorami lub skrzepami krwi, które powstają w płucach, ale przemieszczają się do mózgu, może spowodować udar u osoby z HHT, która ma AVM w płucach.
AVM w płucach można leczyć za pomocą czegoś, co nazywa się embolizacją, w wyniku której blokada jest celowo tworzona w nieprawidłowych naczyniach krwionośnych, chirurgicznie lub może być kombinacją obu technik.
Pacjenci z AVM płuc powinni być regularnie poddawani tomografii komputerowej klatki piersiowej w celu wykrycia wzrostu lub ponownego powstania znanych obszarów wad rozwojowych oraz wykrycia nowych AVM. Badania przesiewowe w kierunku AVM płuc są również zalecane przed zajściem w ciążę, ponieważ zmiany fizjologii matki, które są normalną częścią ciąży, mogą wpływać na AVM.
Aż 70% osób z HHT rozwija AVM w wątrobie. Często te AVM są ciche i zostaną zauważone tylko przypadkowo, gdy skanowanie zostanie wykonane z innego powodu. W niektórych przypadkach AVM w wątrobie może być jednak poważny i może prowadzić do problemów z krążeniem i sercem, a bardzo rzadko do niewydolności wątroby wymagającej przeszczepu.
AVM u osób z HHT powodują problemy w mózgu i układzie nerwowym tylko w około 10-15% przypadków, a problemy te zwykle pojawiają się u osób starszych. Znowu jednak istnieje możliwość wystąpienia ciężkości, przy czym AVM mózgu i kręgosłupa mogą powodować niszczący krwotok, jeśli pękną.
Kogo to dotyczy?
HHT jest chorobą genetyczną przenoszoną z rodziców na dzieci w sposób dominujący, więc każdy może ją odziedziczyć, ale występuje stosunkowo rzadko. Częstotliwość jest podobna zarówno u mężczyzn, jak iu kobiet.
Ogólnie rzecz biorąc, szacuje się, że występuje u około 1 na 8000 osób, ale w zależności od pochodzenia etnicznego i uwarunkowań genetycznych wskaźniki mogą być znacznie wyższe lub znacznie niższe. Na przykład opublikowane wskaźniki rozpowszechnienia wśród osób pochodzenia afro-karaibskiego na Antylach Holenderskich (wyspy Aruba, Bonaire i Curaçao) mają jedne z wyższych wskaźników, szacując je na 1 na 1331 osób, podczas gdy w najbardziej na północ wysuniętych krańcach Anglii stawki szacuje się na 1 na 39 216.
Diagnoza
Kryteria diagnostyczne Curaçao, nazwane na cześć wyspy karaibskiej, odnoszą się do schematu, który można wykorzystać do określenia prawdopodobieństwa wystąpienia HHT. Zgodnie z kryteriami rozpoznanie HHT to określony jeżeli spełnione są 3 z poniższych kryteriów, możliwe lub podejrzane jeśli 2 są obecne i mało prawdopodobne jeśli jest mniej niż 2:
- Spontaniczne, nawracające krwawienia z nosa
- Teleangiektazje: liczne, pająkowate plamy żylne w charakterystycznych miejscach - na ustach, w jamie ustnej, na palcach i na nosie
- Teleangiektazje wewnętrzne i wady rozwojowe: teleangiektazje przewodu pokarmowego (z krwawieniem lub bez) i malformacje tętniczo-żylne (płuca, wątroba, mózg i rdzeń kręgowy)
- Historia rodziny: krewna pierwszego stopnia z dziedziczną teleangiektazją krwotoczną
Rodzaje
Według przeglądu Kroona i współpracowników z 2018 roku na ten temat znanych jest 5 typów genetycznych HHT i jeden połączony zespół polipowatości młodzieńczej i HHT.
Tradycyjnie opisano 2 główne typy: Typ I jest związany z mutacjami w genie zwanym endoglingen. Ten typ HHT ma również wysokie wskaźniki AVM w płucach lub płucnych AVM. Typ 2 jest związany z mutacjami w genie zwanym gen kinazy podobnej do receptora aktywiny-1 (ACVRL1). Ten typ ma niższe wskaźniki AVM płuc i mózgu niż HHT1, ale wyższy wskaźnik AVM w wątrobie.
Mutacje w genie endogliny na chromosomie 9 (HHT typ 1) oraz w genie ACVRL1 na chromosomie 12 (HHT typ 2) są związane z HHT. Uważa się, że te geny odgrywają ważną rolę w rozwoju organizmu i naprawie naczyń krwionośnych. Nie jest to jednak tak proste, jak 2 geny, ponieważ nie wszystkie przypadki HHT powstają z tych samych mutacji. Większość rodzin z HHT ma unikalną mutację. Według badań Prigody i współpracowników, obecnie potencjalnie datowanych, zgłoszono 168 różnych mutacji w genie endogliny i 138 różnych mutacji ACVRL1.
Oprócz endogliny i ACVRL1 z HHT powiązano kilka innych genów. Mutacje w genie SMAD4 / MADH4 są związane z połączonym zespołem czegoś, co nazywa się polipowatością młodzieńczą i HHT. Zespół polipowatości młodzieńczej lub JPS jest schorzeniem dziedzicznym identyfikowanym przez obecność nienowotworowych narośli lub polipów w przewodzie pokarmowym, najczęściej w okrężnicy. Rozrosty mogą również wystąpić w żołądku, jelicie cienkim i odbytnicy. Tak więc w niektórych przypadkach ludzie mają zarówno zespół HHT, jak i zespół polipowatości, co wydaje się być związane z mutacjami genu SMAD4 / MADH4.
Monitorowanie i zapobieganie
Oprócz leczenia teleangiektazji i AVM w razie potrzeby, ważne jest, aby osoby z HHT były monitorowane, niektórzy uważniej niż inni. Doktor Grand’Maison zakończył dokładny przegląd HHT w 2009 r. I zaproponował ogólne ramy monitorowania:
Corocznie należy sprawdzać obecność nowych teleangiektazji, krwawień z nosa, krwawień z przewodu pokarmowego, objawów ze strony klatki piersiowej, takich jak duszność lub odkrztuszanie krwi, oraz objawów neurologicznych. Co roku należy również sprawdzać krew w stolcu, podobnie jak pełną morfologię krwi w celu wykrycia anemii.
Zaleca się, aby co kilka lat w dzieciństwie wykonywać pulsoksymetrię w celu wykrycia AVM płuc, a następnie obrazować, jeśli poziom tlenu we krwi jest niski. W wieku 10 lat zaleca się badanie układu sercowo-naczyniowego w celu wykrycia poważnych AVM, które mogą wpływać na zdolność serca i płuc do wykonywania ich pracy.
W przypadku osób z ustalonymi AVM w płucach zalecane monitorowanie jest wykonywane nawet częściej. Badania przesiewowe wątroby w kierunku AVM nie są traktowane priorytetowo, ale można je wykonać, podczas gdy MRI mózgu w celu wykluczenia poważnych AVM jest zalecane przynajmniej raz po postawieniu diagnozy HHT.
Zabiegi badawcze
Bewacyzumab był stosowany jako terapia przeciwnowotworowa, ponieważ jest to terapia głodująca nowotwór lub terapia antyangiogenna; zapobiega rozwojowi nowych naczyń krwionośnych, w tym normalnych naczyń krwionośnych i naczyń krwionośnych odżywiających guzy.
W niedawnym badaniu Steinegera i współpracowników 33 pacjentów z HHT zostało włączonych do badania wpływu bewacyzumabu na osoby z teleangiektazją nosa. Średnio każdy pacjent otrzymał około 6 donosowych wstrzyknięć bewacyzumabu (zakres 1-16) i był obserwowany średnio przez około 3 lata w tym badaniu. Czterech pacjentów nie wykazało poprawy po leczeniu. Jedenastu pacjentów wykazało początkową poprawę (niższe wskaźniki objawów i mniejsza potrzeba transfuzji krwi), ale leczenie przerwano przed końcem badania, ponieważ efekt stawał się stopniowo krótszy pomimo powtarzanych wstrzyknięć. Dwunastu pacjentów nadal miało pozytywną odpowiedź na leczenie pod koniec badania.
Nie zaobserwowano żadnych miejscowych działań niepożądanych, ale u jednego pacjenta wystąpiła martwica kości (choroba kości, która może ograniczać aktywność fizyczną) w obu kolanach w okresie leczenia. Autorzy doszli do wniosku, że donosowe wstrzyknięcie bewacyzumabu jest skutecznym sposobem leczenia większości umiarkowanych i ciężkich krwawień z nosa związanych z HHT. Czas trwania efektu leczenia był jednak różny u każdego pacjenta, a rozwój oporności na leczenie wydawał się dość powszechny.
Ekranizacja
Badania przesiewowe w kierunku tej choroby to ewoluująca dziedzina. Ostatnio Kroon i współpracownicy zaproponowali systematyczne badania przesiewowe pacjentów z podejrzeniem HHT. Zalecają zarówno kliniczne, jak i genetyczne badanie przesiewowe pacjentów z podejrzeniem HHT w celu potwierdzenia diagnozy i zapobiegania powikłaniom związanym z HHT.